Una modificación del genoma del VIH puede dar un giro al diseño de la vacuna
Investigadores han descubierto que la infección por VIH de las células inmunes humanas provoca un aumento masivo de la metilación
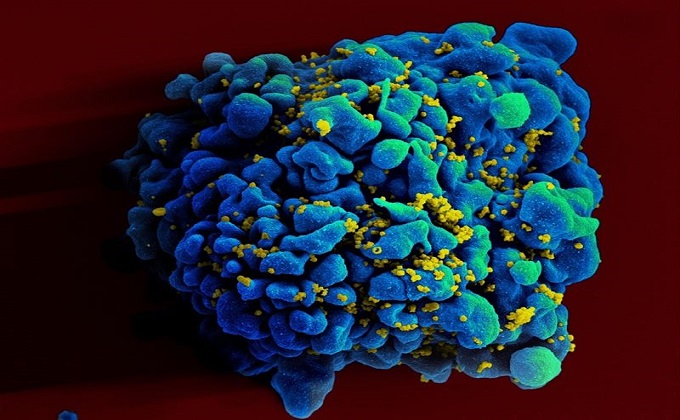
Investigadores de la Escuela de Medicina de la Universidad de California, San Diego, Estados Unidos, han descubierto que la infección por el virus de la inmunodeficiencia humana (VIH) de las células inmunes humanas provoca un aumento masivo de la metilación, una modificación química, tanto en el ARN viral como humano y, ayudar a la replicación del virus.
El trabajo, publicado este lunes en 'Nature Microbiology', identifica un nuevo mecanismo para el control de la replicación del VIH y su interacción con el sistema inmune del huésped.
"Nosotros y otros colegas en las compañías farmacéuticas han trabajado durante años para desarrollar fármacos dirigidos al material genético del VIH, su ARN, pero nunca han llegado a la clínica", explica el autor principal de este estudio, Tariq Rana, profesor de Pediatría en la Escuela de Medicina de la Universidad de California de San Diego. "Ahora sabemos por qué: estábamos desarrollando fármacos a partir de dianas de ARN que no tienen estas modificaciones, cuando en realidad el ARN era diferente", añade.
En las células humanas, el ARN es el material genético que lleva instrucciones desde el ADN en el núcleo de una célula fuera del citoplasma, donde la maquinaria molecular utiliza esas instrucciones para construir proteínas. Por el contrario, el genoma completo del VIH se compone de ARN, no de ADN. El virus secuestra la maquinaria celular del huésped para traducir su ARN a las proteínas.
Las células pueden modificar químicamente el ARN para controlar o alterar su función. Una de estas modificaciones, M6A, es común en los seres humanos y otros organismos pero se sabe poco sobre el papel que M6A juega en el sistema inmunológico humano o en las interacciones entre las células y los patógenos invasores, como el VIH.
En su investigación, el equipo de Rana descubrió modificaciones M6A en el ARN del VIH por primera vez y también examinó el efecto de M6A en el trabajo tanto del ARN en el VIH como en el huésped humano durante la infección de las células inmunes humanas.
"Siempre se había considerado M6A como una modificación constante del ARN celular. En cambio, resulta ser extremadamente dinámico y tener gran capacidad de respuesta a los estímulos externos, como infecciones virales", dice Gianluigi Lichinchi, estudiante graduado en el laboratorio de Rana y primer autor del estudio. "En el futuro, estos hallazgos podrían ayudar a mejorar el diseño y la eficacia de las vacunas contra el VIH/sida", augura.
Una de las proteínas codificadas por el genoma de ARN del VIH es Rev. Después de que las proteínas Rev se construyen en el citoplasma de la célula huésped humana, vuelven de nuevo al núcleo, donde se reúnen en un punto particular en el ARN del VIH llamado elemento de respuesta a Rev (RRE, por sus siglas en inglés). Allí, Rev ayuda a transportar transcripciones de ARN del VIH recién producidas en el citoplasma de acogida, un paso esencial para la replicación viral.
El equipo determinó que la modificación M6A tanto de ARN humano como viral influye en la interacción entre la proteína Rev del VIH y RRE del ARN. Cuando los investigadores silenciaron la enzima que elimina M6A a partir del ARN, la replicación del VIH aumentó; mientras quecuando silenciaron la enzima que añade M6A al ARN, la replicación del VIH se redujo, un hallazgo que creen que podría explotarse farmacológicamente para combatir la infección.
"El campo del VIH se ha perdido esta modificación en la estructura fisiológica del ARN y el genoma del VIH durante más de 30 años", señala Rana. "No me sorprendería que otros virus con genomas ARN también exploten este mecanismo de modificación M6A para evadir la vigilancia inmune y controlar su replicación en células humanas. Estos virus incluyen, por ejemplo, la gripe, la hepatitis C, el ébola y Zika, sólo por nombrar algunos", concluye.










